
Инсектоакарициды
Хлорорганические соединения. Физико-химические свойства и применение. Хлорорганические соединения (ХОС) широко применяют в качестве инсектицидов, акарицидов и фунгицидов для борьбы с вредителями зерновых, зернобобовых, технических и овощных культур, лесонасаждений, плодовых деревьев и виноградников, а также используются в медицинской и ветеринарной санитарии для уничтожения зоопаразитов и переносчиков болезней. Выпускают их в виде смачивающихся порошков, минерально-масляных эмульсий, дустов. У нас разрешены для применения следующие препараты: гексахлорциклогексан (ГХЦГ), гамма-изомер ГХЦГ (линдан), гексахлорбутадиен (ГХБД), дилор, мезокс, полихлоркамфен (ПХК), тедион, каптан, тиодан и некоторые другие. Запрещено использовать такие опасные пестициды, как альдрин, дильдрин, эндрин и галекрон, ДДТ. Однако ДДТ пока сохраняет свое значение в карантинных ситуациях. Благодаря резко выраженным кумулятивным свойствам и персистентности он пока циркулирует в объектах внешней среды.
ХОС представляют собой галоидопроизводные многоядерных циклических углеводородов (ДДТ и его аналоги), циклопарафинов (ГХЦГ и его аналоги), соединений диеного ряда (альдрин, дильдрин, гексахлорбутадиен, гептахлор, дилор), терпенов (ПХП и ПХК), бензола и других соединений.
Все ХОС плохо растворяются в воде и хорошо в органических растворителях, маслах и жирах. Причем в пресной воде растворимость их выше, чем в соленой (эффект "высаливания"). В водоемах они поглощаются частицами органических веществ и осадком, вследствие чего их свойства и локализация могут меняться в разных типах водоемов. В акваториях, загрязненных нефтью, возникает опасность концентрирования ХОС в пленке, растворимых фракциях и в донном осадке.
ХОС обладают высокой химической стойкостью к воздействию различных факторов внешней среды, относятся к группе высокостабильных и сверхвысокостабильных пестицидов. В почве ДДТ сохраняется 12 и более лет, ПХП и ПХК - до 0,5-2 лет, линдан и кельтан - до одного года. Коэффициент выноса ХОС из почвы с поверхностным стоком составляет для ДДТ 0,02-0,3%, ГХЦГ - 0,06-0,10%, что соответствовало концентрации в воде 0,03- 0,3 мкг/л (Ц. И. Бобовникова и др.). Обладая этими свойствами, ХОС накапливаются в гидробионтах и передаются по пищевой цепи, увеличиваясь примерно на порядок в каждом последующем звене. Однако не все препараты обладают одинаковой персистентностью и кумулятивными свойствами. В гидросфере и организме гидробионтов они постепенно разлагаются с образованием метаболитов. По вышеназванным причинам в зонах интенсивного земледелия остатки ХОС и метаболитов в организме гидробионтов обнаруживаются постоянно, что следует учитывать при диагностике отравлений.
В пресных и морских водоемах, а также гидробионтах, помимо хлорорганических пестицидов, встречаются сходные с ними полихлорированные бифенилы (ПХБФ) и терфенилы (ПХТФ), используемые в промышленности. По своим физико-химическим свойствам и физиологическому действию на организм, а также методам анализа они весьма близки к хлорорганическим пестицидам. Поэтому необходима дифференциация этих групп хлорированных углеводородов.
Токсичность. Механизм действия ХОС на рыб во многом сходен с их влиянием на теплокровных животных. Рыбы и другие водные организмы более чувствительны к ХОС, чем наземные животные. Особенно чувствительны к ХОС водные ракообразные и насекомые, которых нередко используют для контроля загрязнения воды как индикаторные организмы.
В организм рыб ХОС поступают осмотически через жабры и через пищеварительный тракт с кормом. Интенсивность поглощения ХОС рыбами увеличивается при повышении температуры воды. Гидробионты способны концентрировать ХОС в гораздо больших количествах, чем в окружающей среде (воде, грунте), коэффициент накопления этих веществ составляет в грунте 100, зоопланктоне и бентосе - 100-300, рыбах - 300-3000 и более. По этому показателю они относятся к группе веществ со сверхвысокой или с выраженной кумуляцией. Суммарные концентрации ХОС в воде пресных и морских водоемов обычно ниже микрограмма на литр.
В первую очередь ХОС накапливаются в органах и тканях, богатых жирами или липоидами. У рыб их больше всего находят во внутреннем жире, головном мозге, желудочной и кишечной стенке, гонадах и печени, меньше - в жабрах, мышцах, почках и селезенке. С возрастом рыб отмечено увеличение концентрации ХОС. При метаболизме жиров во время голодания и миграции рыб, а также при стрессовых состояниях накопленные в организме ХОС могут вызвать отравления рыб.
ХОС относят к ядам политропного действия с преимущественным поражением центральной нервной системы и паренхиматозных органов, особенно печени. Кроме того, они вызывают расстройство функций эндокринной и сердечнососудистой системы, почек и других органов. ХОС также резко угнетают активность ферментов дыхательной цепи, нарушают тканевое дыхание. Некоторые препараты блокируют SH-группы тиоловых ферментов. ХОС опасны для рыб своими отдаленными последствиями: эмбриотоксическим, мутагенным и тератогенным действием. Они снижают иммунологическую реактивность и повышают восприимчивость рыб к инфекционным болезням. ХОС относятся к группе высокотоксичных для рыб соединений (табл. 30).

Таблица 30. Токсичность основных хлорорганических пестицидов для рыб
* (Абсолютно смертельные концентрации (CK100).)
** (Концентрация по препарату.)
Хроническое отравление карпов ПХК и полидофеном наступает при концентрациях до 1/100 от CK50 (0,004 мг/л), кельтаном до 1/300 от CK50 (0.007 мг/л) и сопровождается гибелью 10-60% рыб в течение 60-80 дней воздействия. Токсические концентрации других препаратов не установлены. На основании изучения экспериментальных и природных токсикозов у погибших рыб обнаружены остатки некоторых ХОС (табл. 31).
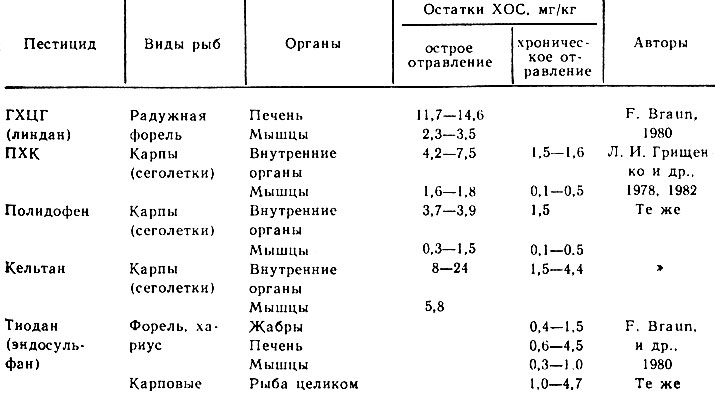
Таблица 31. Содержание ХОС в органах рыб после отравления
В органах рыб, перенесших отравление, остатки ПХК, полидофена и кельтана обнаруживают до 50 дней, а в трупах рыб до 8. При хранении погибших рыб в холодильнике они сохраняются в тканях около 4 мес.
При поступлении ХОС с кормом интоксикация наступает при достижении летального уровня их содержания в органах рыб, что доказано на экспериментальной модели кумулятивного токсикоза (Ф. Я. Комаровский и др.).
В естественных условиях уровень накопления ХОС в рыбах зависит от объема применения и величины остатков пестицидов в сточных водах. В зонах с умеренным применением хлорорганических пестицидов их остатки во внутренних органах рыб составляют: планктонофагов (плотва, тюлька) - 0,01 - 0,5 мг/кг и хищников (судак, окунь, щука) - 0,2-2,5 мг/кг. В жировых отложениях возможно увеличение на 1-2 порядка.
Из представителей зоопланктона наиболее чувствительны к ХОС водные членистоногие и ракообразные. Токсические концентрации для дафний находятся на уровне 0,001 мг/л, циклопов - более 0,01 мг/л. В то же время простейшие, моллюски, хирономиды к ним довольно устойчивы.
Симптомы и патоморфологические изменения. Несмотря на различие в химической структуре, картина отравлений рыб хлорорганическими пестицидами однотипна. В первую очередь они действуют на рыб как нервные яды.
Сроки появления признаков отравления зависят от величины концентраций препаратов и времени их воздействия. При остром отравлении они наступают через несколько часов после начала контакта с ядом, а при хроническом - через 7-10 дней.
Наиболее бурно симптомы проявляются при остром отравлении и характеризуются они повышенной возбудимостью, резким повышением подвижности рыб, отсутствием реакции на прикосновение к телу, нарушением координации движения (плавание по кругу, спирали, опрокидывание на бок) и полной потерей равновесия, замедлением дыхания. В агональной стадии развиваются параличи, гибель наступает от паралича центра дыхания. При вскрытии погибших рыб обнаруживают выраженное полнокровие внутренних органов, особенно печени и предсердия, иногда встречаются мелкоточечные кровоизлияния в Жабрах. Гистологическими исследованиями устанавливают застойную гиперемию сосудов печени, почек, головного мозга, зернистое и жировое перерождение, а при высоких концентрациях вакуольную дистрофию печеночных клеток (иногда их некробиоз), токсический отек жаберных лепестков, незначительное Набухание респираторного эпителия.
При хроническом отравлении рыбы перестают потреблять корм, угнетены или ведут себя беспокойно, интенсивно плавают у поверхности воды, затем они теряют равновесие, перевертываются на бок и погибают в состоянии депрессии. Печень погибших рыб набухшая, увеличена в объеме, с бледноватым оттенком. Отравление сопровождается тяжелыми дистрофическими и некробиотическими изменениями во внутренних органах и головном мозге. В печени обнаруживают обширные очаги зернисто-жировой и водяночной дистрофии, а также фокусы некробиоза печеночных клеток, снижение или отсутствие в них гликогена. Иногда в печени отмечают гипертрофию клеток с наличием в них митотических фигур деления, а также скопление в их цитоплазме липофусцина.
В почках - дистрофия и последующая деструкция эпителия канальцев. Отмечена дистрофия и некробиоз клеток гемопоэтической ткани.
При высоких концентрациях препаратов жаберные лепестки отечны, респираторный эпителий набухший, отслоен от мембраны, частично десквамирован. При низких концентрациях эти изменения слабо выражены. Постоянно отмечают дистрофию нейронов головного мозга и инволюцию фолликулярного эпителия в яичниках.
В случаях острого и особенно хронического отравления устанавливают снижение уровня гемоглобина и количества эритроцитов (на 10-20%), лейкопению (число лейкоцитов снижено на 60%), нейтрофилию, лимфоцитопению. В эритроцитах отмечена гипохромазия, анизоцитоз, пойкилоцитоз, макро- и микроцитоз.
При поступлении пестицидов с кормом обнаруживают десквамативный катар кишечника, застойную гиперемию и дегенеративно-некробиотические изменения в печени.
Диагноз ставят на основании комплексных исследований; анамнестических данных, клинико-анатомической картины интоксикации и обнаружения пестицидов в воде, грунте, органах рыб и других гидробионтах. Хлорорганические пестициды в этих объектах определяют газохроматографическим методом согласно "Методическим указаниям по определению ХОП и ПХБ при их совместном присутствии в объектах внешней среды и биоматериале", утвержденным Минздравом СССР. Для определения ПХК, полидофена и кельтана в воде и органах рыб разработаны и утверждены ГУВ Госагропрома СССР методы тонкослойной хроматографии.
Прямым доказательством отравления рыб служат обнаружение ХОС в воде и органах рыб на уровне вышеприведенных летальных показателей и наличие клинико-анатомических признаков интоксикации. В сомнительных случаях данные химического анализа необходимо сравнивать с остатками ХОС в органах рыб из благополучных водоемов. В рыбах и других объектах из крупных естественных водоемов дополнительно определяют содержание полихлорбифенилов.
Профилактика заключается в недопущении внесения ХОП в водоохраной зоне, склоновых участках и основной водосборной площади водоемов, соблюдении правил применения, хранения, транспортирования и утилизации пестицидов, периодическом контроле их остатков в воде, грунте, гидробионтах. Присутствие ХОС в воде рыбохозяйственных водоемов не допускается. Допустимые остаточные количества гексахлорана (сумма изомеров) в рыбе 0,2 мг/кг, ДДТ в рыбе и рыбных консервах 0,2 мг/кг (временно), ПХК и ПХП не допускаются, для остальных ХОС не установлены.
Рыба, содержащая остатки хлорорганических пестицидов, реализуется согласно санитарно-гигиеническим правилам.
Полихлорированные бифенилы и терфенилы (полихлорбифенилы, ПХБ, ПХБФ, ПХТФ). Полихлорбифенилы, выпускаемые примерно с 1930 г., широко применяются в качестве пластификаторов (для лаков и красок, клеев, замазок и пластмасс), теплоносителей, диэлектриков в трансформаторах и конденсаторах, а также добавок к некоторым пестицидам для снижения их летучести. Они известны под различными торговыми названиями: арохлор, фенохлор, канехлор, хлорфен, совол (СССР). Химический состав серии "арохлор" шифруется четырехзначным кодом, в котором первой цифрой 12 обозначаются бифенилы, а последующими двумя цифрами - процент содержания хлора по массе. Например, арохлор 1260 представляет собой смесь ПХБФ, содержащих 60% хлора.
Главным источником загрязнения пресноводных и морских водоемов полихлорбифенилами являются промышленные сточные воды. Повышенное содержание их в воде и рыбе отмечено в ряде крупных морских и пресноводных бассейнов, находящихся вблизи промышленных центров. Полихлорбифенилы устойчивы в окружающей среде, малорастворимы в воде, концентрируются в иловых отложениях водоемов, небольшая часть их подвергается биотрансформации микроорганизмами и водорослями. Особенно устойчивы высокохлорированные соединения. В силу этого они обладают высокой степенью материальной кумуляции и передаются по трофической цепи.
Считают, что незагрязненные пресные воды содержат менее 0,5 нг/л ПХБФ, в умеренно загрязненных реках обнаруживают около 50 нг/л и сильно загрязненных - 500 нг/л. Высокие концентрации ПХБФ, превышающие их растворимость в воде, объясняют адсорбцией ПХБФ взвешенными частицами.. Уровень накопления в живых организмах зависит от степени локального загрязнения, содержания жира в тканях и места гидробионтов в трофической цепи. Он повышается от планктофагов и бентофагов до хищников.
В слабо загрязненных водоемах содержание ПХБФ в мышечной ткани разных рыб, употребляемых в пищу, составляло около 0,1 мг/кг при колебании от 0,01 до 0,48 мг/кг (сельдь, треска). В зонах умеренного и сильного загрязнения их уровень в мышечной ткани рыб превышал 0,5 мг/кг и в экстрагируемом жире 1,0-3,9 мг/кг, а в мясе рыбоядных птиц 17-18 мг/кг (420- 650 мг/кг в экстрагируемом жире).
Токсичность ПХБ для гидробионтов изучена недостаточно. Считают, что они близки по своему действию к хлорорганическим соединениям. Изменяется токсичность ПХБ в зависимости от их состава, степени хлорирования, наличия примесей и др. В организм рыб ПХБФ могут поступать осмотически через жабры, но основная часть их потребляется с кормом. Они накапливаются в первую очередь в жировой ткани, печени и головном мозге и меньше во внутренних органах.
Сведения об острой токсичности ПХБФ при осмотическом поступлении малочисленны. Среднесмертельная концентрация арохлора 1242 и 1254 для мальков черноголовой пимефалес составила при экспозиции 4-5 сут 8 мкг/л, радужной форели и ушастого окуня-137-156 мкг/л. Хроническое отравление радужной форели наступало при концентрации 8 мкг/л через 10 дней, ушастого окуня - 54 мкг/л через 25 дней, канального сома - 57 мкг/л через 15 дней, розовой креветки - 5 мкг/л через 20 дней.
При скармливании арохлора 1254 форели в дозе 10 и 100 мг/кг в течение 330 дней наблюдались патологические изменения в почках, селезенке и печени. У карпов, получавших 0,25 мг/кг арохлора 1248 в течение 21 дня, отмечена глобулинемия, уменьшение активности лизосомальных и микросомальных ферментов печени и повышение активности глюкоронидазы и других ферментов дыхательного цикла.
Хроническое действие ПХБ при употреблении загрязненной рыбы и других продуктов опасно для теплокровных животных и человека. В Японии зарегистрированы случаи отравления людей (болезнь Юшо) и цыплят (бройлеров) рисовым маслом, загрязненным полихлорбифенилами. Случаи отравления загрязненной рыбой не зарегистрированы.
Симптомы и патоморфологические изменения изучены слабо. Кроме вышеперечисленных изменений, при скармливании карпам арохлора 1254 обнаруживали жировую дистрофию в печени, некробиоз сперматогенного эпителия в семенниках, а также гиперплазию респираторного эпителия жабр.
Диагноз ставится комплексно с обязательным определением ПХБФ в воде и рыбе газохроматографическим методом, приведенным в разделе "Хлорорганические соединения".
Профилактика основывается на строгой регламентации поступления ПХБФ в водоемы. Присутствие ПХБФ в воде морских рыбохозяйственных водоемов не допускается, для пресноводных водоемов ПДК не установлена. Допустимые остаточные количества ПХБФ в рыбных продуктах не установлены, но следует учитывать, что для человека опасно потребление ПХБФ в дозе 0,07 мг/кг массы тела в день или суммарной дозе 4,2 мг (критерии ВОЗ, 1980).
Фосфорорганические пестициды (ФОП). Физико-химические свойства. Фосфорорганические соединения (ФОС)-это большая группа пестицидов различного назначения (акарицидов, инсектицидов, фунгицидов, нематоцидов, гербицидов, дефолиантов). Для борьбы с эктопаразитами рыб используют хлорофос и карбофос, остальные попадают в водоемы такими же путями, как ХОП.
Фосфорорганические соединения, за исключением некоторых (хлорофос), плохо растворимы в воде и хорошо - в органических растворителях. Концентраты эмульсий переходят в воде в стойкую эмульсию и наиболее опасны для рыбоводства. ФОС относительно малостойки в окружающей среде. Большая часть их разлагается в растениях, почве и воде в течение одного или нескольких месяцев. Только некоторые инсектоакарициды внутрирастительного действия (метилмеркаптофос, антио, фосфамид, сайфос и др.) сохраняются до года. С увеличением рН и повышением температуры воды скорость гидролиза этих соединений возрастает в несколько раз. В рыбохозяйственных водоемах они, как правило, обнаруживаются в незначительных количествах. Однако при постоянном поступлении со сточными водами, а также в районах массового их применения отмечен довольно высокий уровень ФОС в воде, а также зарегистрированы случаи отравления рыб.
Токсичность. На организм рыб фосфорорганические пестициды действуют примерно так же, как на теплокровных животных. Они угнетают активность фермента нервной системы ацетилхолинэстеразы (АХЭ) и других эстераз, что приводит к накоплению в нервных синапсах ацетилхолина, который вызывает картину отравления. Действие ФОС на центральную нервную систему сопровождается дистрофическими изменениями и гибелью нервных клеток в результате гипоксии. ФОС вызывают нарушения и в других системах.
В организм рыб они поступают в основном осмотически через жабры и частично кожу, распределяются по всем органам и тканям, концентрируясь в наибольших количествах во внутренних органах (печени, почках, стенке кишечника, селезенке). В процессе метаболизма ФОС в органах рыб могут образовываться более токсичные метаболиты, которые следует учитывать при оценке токсичности этих препаратов. Например, хлорофос превращается в более токсичный диметилдихлорвинилфосфат (ДДВФ), карбофос - молооксон, метилмеркаптофос - сульфаксид и сульфон.
Способность к материальной кумуляции у ФОС выражена слабее, чем у ХОС. Однако они обладают функциональной кумуляцией и поэтому могут вызывать хронические отравления.
Наиболее токсичны для рыб производные фосфорной кислоты. Остротоксические концентрации ДДВФ (дихлорофоса) при 24 ч экспозиции составляют для форели 0,5, карпа-1, молоди севрюги - 1 мг/л. Среднесмертельные концентрации гардоны (винфоса) для карпа, толстолобика и буффало находятся в пределах 5,6-6,4; окуня и верховки 3,0-3,6 мг/л ДВ. Содержание гардоны в паренхиматозных органах карпа составляет в среднем 16,0 мг/кг, в мышцах - 2,7 мг/кг. Хроническое отравление карпов наступает в течение 30-40 дней при 1/2-1/5 от CK50 (2,8-1,1 мг/л) и содержании гардоны в органах 6,6 мг/кг. Оба вида отравления и действие сублетальных концентраций сопровождаются угнетением активности АХЭ крови на 80-90%.
Производные тиофосфорной кислоты менее токсичны, чем фосфорной (табл. 32).

Таблица 32. Токсичность фосфорорганических пестицидов (производных тиофосфорной кислоты) для рыб
*(Абсолютно смертельные концентрации (СК100).)
Содержание препаратов в органах рыб при остром отравлении обычно превышает токсические концентрации их в воде в 5-10 раз (Кн-5-10). Токсические концентрации, вызывающие хроническое отравление рыб, составляют примерно 1/3-1/5 от CK50 соответствующего пестицида. Однако они известны не для всех препаратов. В частности, метилнитрофос вызывает частичную гибель карпов в течение 30 дней в концентрации 5,1 мг/л, а ТХМ-3 за 9-11 дней - в концентрации 22,0 мг/л. Более низкие концентрации (до 1/30 от CK50) вызывают угнетение активности АХЭ, гипергликемию, дистрофические изменения в печени и др. Препараты обладают функциональной кумуляцией,, а метафос способен к накоплению (Кн-220).
Производные дитиофосфорной кислоты обладают разной токсичностью для рыб (табл. 33).
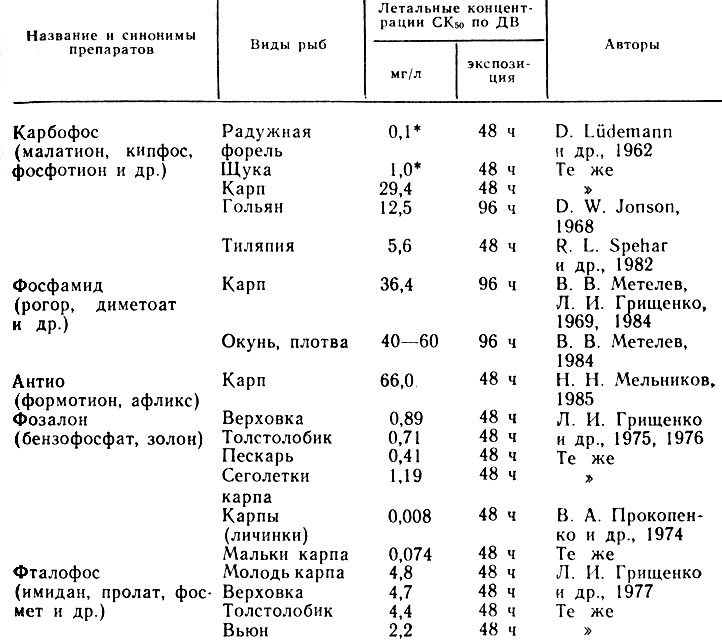
Таблица 33. Токсичность производных дитиофосфорной кислоты для рыб
* (Абсолютно смертельные концентрации (СК100).)
При остром отравлении в органах карпов обнаружено: фозалона 8 - 13 мг/кг, фталофоса-10-16 мг/кг, что превышает их концентрации в воде в 3-10 раз (Кн-3-10).
Хроническое отравление сеголетков карпа наступает через 20-30 суток при концентрациях: фосфамида - 13,5 мг/л, фозалона - 0,36-0,24 мг/л и фталофоса - 0,96-0,48 мг/л, что соответствует 1/3-1/10 от CK50- В этих случаях в органах карпов обнаруживается: фозалона-1,8-4,3 мг/кг, фталофоса - 2,7 мг/кг. Из организма рыб фозалон и фталофос выделяются через 7-9 дней.
Способность к материальной кумуляции наиболее выражена у метафоса, остальные препараты обладают слабыми кумулятивными свойствами. Однако все они способны к функциональной кумуляции, которая проявляется резким угнетением активности АХЭ, крови и головного мозга и длительным восстановлением ее до исходного уровня (через 20-30 дней) после интоксикации.
Из производных фосфоновых кислот наиболее изучено токсическое действие на рыб хлорофоса (диптерекса, негувона), широко применяющегося в сельском хозяйстве и других отраслях.
Остротоксические концентрации хлорофоса (CK50 через 48 ч) для чувствительных рыб - форели, щуки, окуня - составляют 0,75-1,0 мг/л, а для карповых они более высокие: для карпа - 100 мг/л, плотвы - 300, гольяна - 180 мг/л. Дафнии и водоросли погибают при концентрации 0,5 мг/л через 24 ч
При хроническом воздействии смертельные концентрации хлорофоса находятся в следующих пределах: для пеляди - 0,03 мг/л, трехиглой колюшки 0,25 и карпа 2,0 мг/л в течение 25 дней, а для форели - 0,06 мг/л в течение трех месяцев. Дафнии погибают при концентрации 0,005 мг/л и бокоплавы при 0,5 мг/л в течение 25-88 сут.
Содержание хлорофоса в органах карпов при 30-дневном воздействии составило 1,4 мг/кг.
Симптомы и патоморфологические изменения. Признаки отравлений рыб фосфорорганическими пестицидами отличаются только некоторыми особенностями в зависимости от препарата. С повышением концентрации и увеличением экспозиции воздействия интенсивность их проявления усиливается. Для отравлений рыб ФОС характерен нервнопаралитический синдром, местнораздражающее действие слабо выражено.
Острое отравление характеризуется постепенным переходом от фазы возбуждения рыб с наличием судорог и мышечных фибрилляций к резкому угнетению и параличам. Возбуждение проявляется беспокойством, стремительным движением и повышенной чувствительностью рыб к звуковым и тактильным раздражителям. Затем наступает расстройство координации движений и ориентации рыб в воде. Рыбы перевертываются на бок, плавают по кругу или спирали, пятятся назад, принимают диагональное положение. Реакция на звук и прикосновение к телу проявляется толчкообразным движением, тремором плавников и спастическим изгибом всего тела. При длительных спазмах туловище рыб со временем искривляется. Этот признак отмечен при действии фталофоса, хлорофоса, ДДВФ и китацина. В конечной стадии интоксикации наступает депрессия, адинамия и паралич, замедляется частота и нарушается ритм дыхания. Рыбы не берут корм, в результате усиленной перистальтики кишечника в воду выбрасывается его содержимое в виде шнуров.
Хроническое отравление проявляется аналогичными признаками, которые возникают в более отдаленные сроки (через 10-15 дней) и слабее выражены. Искривления туловища становятся необратимыми. Рыбы не питаются, худеют вплоть до истощения.
Острое и хроническое отравление сопровождается резким угнетением активности АХЭ крови и мозга. При тяжелой степени отравления активность АХЭ снижается на 80-90%, при средней - на 60-70% и легкой - на 40- 50%. Отмечают также снижение гликогена в печени, гипергликемию, слабую анемию и стойкую лейкопению.
Патологоанатомические изменения в органах отравленных рыб недостаточно специфичны. При остром отравлении внешние покровы ослизнены, жабры интенсивно розовые или бледные без видимых повреждений. Внутренние органы, особенно печень, кровенаполнены, печень темно-красного или синюшного цвета, дряблой консистенции, предсердие перенаполнено кровью, кишечник пустой. При высоких концентрациях ощущается запах ФОС от внутренних органов. У верховок при интоксикации фозалоном и фталофосом отмечена сильная гиперемия хвостовой вены, которая видна в виде кроваво-красного тяжа.
Микроскопические изменения наиболее выражены в печени, головном мозге, жабрах и почках. В жабрах отмечают отек и утолщение лепесточков, набухание и отслоение респираторного эпителия, а также гипертрофию слизистых клеток. В редких случаях, особенно при воздействии ТХМ-3 и метилнитрофоса, наблюдается очаговый распад и десквамация эпителия. Межбалочные капилляры печени расширены, кровенаполнены, в паренхиме встречаются фокусы диссоциации печеночных клеток, зернистая или вакуольно-жировая дистрофия и некробиоз клеток. Сосуды мозговых оболочек и вещества мозга кровенаполнены, обнаруживают перицеллюлярный и иногда периваскулярный отек, сильное сморщивание и деформацию нейронов, гиперхромность их цитоплазмы и кариопикноз. Изменения в почках ограничиваются расширением сосудов и иногда очаговыми геморрагиями, незначительным отеком сосудистых клубочков, зернистой дистрофией эпителия канальцев и скоплением в их просвете эозинофильных белковых масс. В гемопоэтической ткани почек и паренхиме селезенки отмечают некробиоз кроветворных элементов. В миокарде наблюдается дистрофия мышечной ткани, теряется поперечная исчерченность ткани.
Хроническое отравление сопровождается резким исхуданием или истощением рыб, анемией органов, иногда гидратацией мускулатуры и атрофией печени. Отравление может осложняться эктопаразитарными болезнями и сапролегниозом. В гистологической картине более выражен токсический отек жабр, некробиоз печеночных клеток, атрофия гемопоэтической ткани. При воздействии некоторых препаратов в селезенке и островках поджелудочной железы увеличено количество гемосидероцитов.
Диагноз. Помимо общих принципов, изложенных ранее, при диагностике отравлений рыб ФОС используют специальные методы. Одним из них является определение активности АХЭ в крови или головном мозге отравленных рыб, позволяющий осуществлять групповую диагностику интоксикаций. Однако следует помнить, что угнетение АХЭ вызывают и некоторые другие пестициды, например карбаматы.
Количество большинства ФОС в воде, грунте и органах рыб определяют методами тонкослойной или газо-жидкостной хроматографии, утвержденными ГУВ Госагропрома или Минздравом СССР.
Химические исследования на наличие ФОС следует проводить как можно раньше, но не позднее чем через 3-5 дней. Материал не консервируют, а хранят на льду или в холодильнике.
Профилактика см. общую характеристику пестицидов. Содержание актел-лика, байтекса, базудина, дурсбана, изофоса, метафоса, ДДВФ, карбофоса, фозалона, метилнитрофоса и этафоса в воде рыбохозяйственных водоемов не допускается. ПДК антио - 0,0025 мг/л, сайфоса - 0,0002 и фосфамида - 0,0014 мг/л. ПДК остальных ФОС не установлены.
Производные карбаминовых кислот. Физико-химические свойства и применение. В сельском хозяйстве широко используются производные карбаминовой, тио- и дитиокарбаминовой кислот, обладающие разнообразными пестицидными свойствами. Среди карбаматов имеются эффективные инсектоакарициды (севин, байгон, дикрезил), гербициды (бентиокарб, хлор-ИФК, тиллам, эптам, ялан, триаллат), фунгициды (карбатион, поликарбацин, ТМТД, цинеб), нематициды и регуляторы роста растений. Они попадают в водоемы при опрыскивании и опыливании растений, а гербициды ялан и бентиокарб - со сбросными водами с рисовых систем, где они широко применяются.
По стойкости во внешней среде карбаматы относятся к средне- и высокостабильным веществам. Разложение их идет быстрее в кислой среде. При разложении производных карбаминовой кислоты образуется изоцианат, анилин, хлоранилин и парааминофенолы; тиокарбаминовой кислоты - меркаптаны и аммиак. Дитиокарбаматы разлагаются с образованием весьма токсичных (H2S, диметиламин, метилизоцианат), а также стойких соединений (тетраметилтиомочевина, этилентиомочевина, этилентиурамдисульфид и др.).
Ялан и эптам в концентрациях 0,5-1,0 мг/л, а тлкже другие карбаматы почти не влияют на гидрохимический режим водоема.
Токсичность карбаматов для рыб и других гидробионтов, за исключением севина, ялана и бентиокарба, изучена недостаточно. На теплокровных животных установлено, что характерным для многих соединений является поражение нервной и кроветворной систем, эндокринных органов. Инсектицидные препараты обладают выраженной антихолинэстеразной активностью. Ряд производных карбаминовой и дитиокарбаминовой кислот оказывает эмбриотоксическое, мутагенное, аллергенное и бластомогенное действия. Ялан и бентиокарб вызывают резкое угнетение гемопоэза и нарушение эмбриогенеза рыб.
Все карбаматы относятся к группе сильно- и умереннотоксичных соединений (табл. 34).

Таблица 34. Токсичность производных карбаминовой, тиокарбаминовой и дитиокарбаминовой кислот
Среднесмертельные концентрации ялана и эптама для дафний находятся в пределах 4,7-7,5 мг/л ДВ, севина - 0,0012 мг/л ДВ.
Хроническое отравление язей, плотвы и карпов наблюдалось при 0,2 мг/л ялана в течение 20 дней. Параллельно с этим происходило уменьшение численности и обеднение видового состава зоопланктона, нарушался овогенез у дафний.
В организме рыб карбаматы распределяются по всем органам, но в наибольших количествах они концентрируются во внутренних органах (селезенке, печени, почках), которые и берут для исследования.
Симптомы и патоморфологические изменения. Клиническая картина острого отравления рыб характеризуется нервнопаралитическими явлениями: угнетением, спазмами и параличами нервно-мышечного аппарата. В начальной стадии отмечают кратковременное возбуждение рыб, затем нарушается координация движений и ритм дыхания. При отравлении севином проявляются признаки асфиксии. Перед гибелью рыбы сильно угнетены, опускаются на дно, движения их резко замедлены. При хроническом отравлении рыбы не питаются, худеют, иногда поражаются сапролегнией.
Отравление севином и бентиокарбом сопровождается умеренным снижением активности АХЭ крови (на 50-60%), анемией, лейкопенией и нейтрофилией, а также дегенерацией эритроцитов (полиморфизм ядер, олигохромазия, образование "клеток-теней").
При патоморфологическом исследовании обнаруживают в жабрах слабый отек лепестков, отслоение и набухание респираторного эпителия; застойную гиперемию во внутренних органах; в печени и эпителии канальцев почек- зернистую дистрофию и некробиоз отдельных клеток; в селезенке - пролиферацию ретикулогистиоцитов, а при хроническом отравлении севином и бентиокарбом- гемосидероз; в нейронах головного мозга - уплотнение цитоплазмы. При хроническом отравлении яланом (0,2 мг/л) отмечено увеличение весового индекса и некрозы в печени, гипохромная анемия, распад эритроцитов и лейкоцитов в периферической крови и гемопоэтической ткани, анемия жабр и паренхиматозных органов.
Диагноз устанавливают комплексно с обязательным определением содержания карбаматов в воде и органах рыб. При подозрении на отравление севином и другими инсектицидами дополнительно уточняют активность АХЭ и качественные изменения в эритроцитах.
Для установления большинства карбаматов в воде, почве и органах рыб используют методы тонкослойной и газожидкостной (бентиокарб и ялан в рыбе) хроматографии. Достоверным указанием на отравление рыб бентио карбом яланом и севином является обнаружение их остатков в воде и внутренних органах, наличие симптомов интоксикации.
Профилактика основана на общих принципах предотвращения поступления ядохимикатов в водоемы. Сточные воды с рисовых систем следует выдерживать в прудах - накопителях до разложения карбанатных гербицидов. Присутствие ТМТД, дециса и эптана в воде рыбохозяйственных водоемов не допускается, ПДК севина лишь 0,0005 мг/л, бентиокарба (сатурна) - 0,0002, ялана - 0,0007 мг/л.
|
ПОИСК:
|
© RIBOVODSTVO.COM, 2010-2022
При использовании материалов сайта активная ссылка обязательна:
http://ribovodstvo.com/ 'Рыбоводство'
При использовании материалов сайта активная ссылка обязательна:
http://ribovodstvo.com/ 'Рыбоводство'